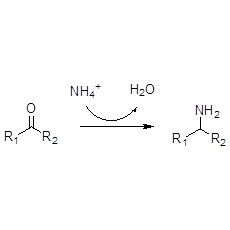
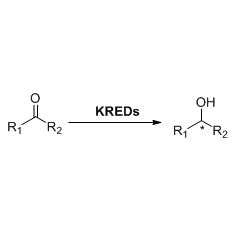
Энередуктаза (ERED)
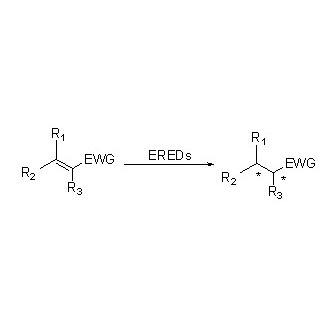
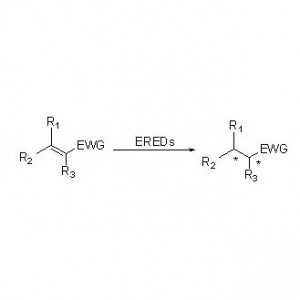
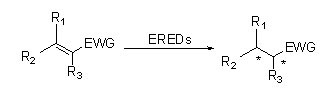
ES-EREDs катализируют реакции с различными типами субстратов благодаря широкому спектру субстратов. В целом, связи C=C α,β-ненасыщенных соединений с электронопоглощающими группами (включая кетоновые альдегиды, нитрогруппы, карбоновые кислоты, сложные эфиры, ангидриды, лактоны, имины и т. д.) легко восстанавливаются ES-EREDs, тогда как неактивированные двойные связи — нет.
Компания SyncoZymes разработала 46 видов ферментных продуктов ERED (с номерами от ES-ERED-101 до ES-ERED-146).
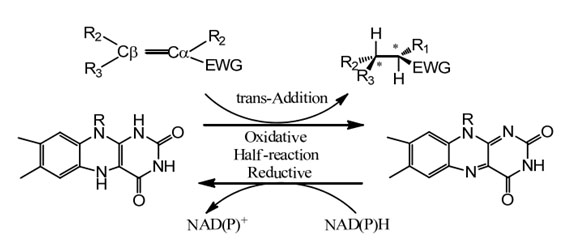
Каталитический механизм:
| Ферменты | Код товара | Спецификация |
| Ферментный порошок | ES-ERED-101~ ES-ERED-146 | Набор из 46 енредуктаз, по 50 мг каждая, 46 штук * 50 мг/штука, или другое количество. |
| Набор для скрининга (SynKit) | ES-ERED-4600 | Набор из 46 енредуктаз, по 50 мг каждая, 46 штук * 50 мг/штука, или другое количество. |
★ Высокая субстратная специфичность.
★ Высокая хиральная селективность.
★ Высокая конверсия.
★ Меньше побочных продуктов.
★ Мягкие условия реакции.
★ Экологически чистый продукт.
★ Высокий уровень безопасности.
➢ Обычно реакционная система должна включать субстрат, буферный раствор (оптимальный pH реакции), коферменты (NAD(H) или NADP(H)), систему регенерации коферментов (например, глюкозо- и глюкозодегидрогеназу) и ES-ERED.
➢ Все ES-ERED можно протестировать соответственно в описанной выше реакционной системе или с помощью набора для скрининга ERED (SynKit ERED).
➢ Все виды ES-ERED, соответствующие различным оптимальным условиям реакции, следует изучать индивидуально.
➢ Высокая концентрация субстрата или продукта может ингибировать активность ES-ERED. Однако ингибирование можно снять путем периодического добавления субстрата.
Пример 1 (α,β-ненасыщенные альдегиды или кетоны)(1):
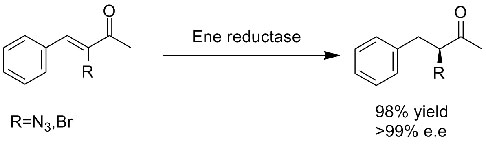
Пример 2 (α,β-ненасыщенные карбоновые кислоты и их производные)(2):
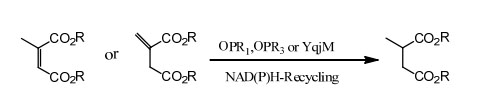
Хранить при температуре ниже -20℃ в течение 2 лет.
Никогда не допускайте контакта с экстремальными условиями, такими как: высокая температура, высокий/низкий уровень pH и высокая концентрация органических растворителей.
1. Лусидио С., Фарделоне Дж., Аугусто Р. и др. J.Mol.Catal.B:Enzym., 2004, 29: 41-45.
2. Stueckler C, Hall M, Ehammer H, et al. .Org.Lett, 2007, 9(26): 5409-5411.